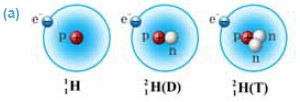
•Protonların sayı eyni, lakin kütlə ədədləri müxtəlif olan atomlar izotoplar adlanır.
Elementlərin dövri sistemində xanalar yük ədədinə görə müəyyən olunduğundan izotoplar eyni bir xanada yerləşir və eyni kimyəvi xassəyə malik olur. Təbiətdə eyni bir kimyəvi elementin iki və ya daha çox izotopu mövcud ola bilər. İzotoplar birbirindən yalnız nüvələrindəki neytronların sayına görə fərqlənir. Neytronlar elementin kimyəvi xassəsinə heç bir təsir göstərmədiyindən eyni elementin bütün izotoplarının kimyəvi xassələri də eyni olur. Məsələn, hidrogenin üç izotopu mövcuddur: 11H (protium) izotopunun nüvəsi yalnız 1 protondan ibarətdir. Onun nüvəsində neytron yoxdur. 21H (deyterium-D) izotopunun nüvəsi bir proton və bir neytrondan ibarətdir. 13H (tritium-T) izotopunun nüvəsi 1 proton və iki neytrondan təşkil olunmuşdur (a). Lakin nüvəsində neytronlarının sayı müxtəlif olan izotoplar müxtəlif fiziki xassəyə malikdir. Məsələn, ağır su – deyterium ilə oksigenin birləşməsi (D2O) adi sudan fərqlənir. Belə ki, normal atmosfer təzyiqində ağır su 101,2°C temperaturda qaynayır və 3,8°C temperaturda isə donur.
• Protonlarının sayı eyni, kütlə ədədləri müxtəlif olan atomlar izotoplar (yun. “izos” – eyni + “topos” – yer) adlanır.