| – | Əhəngdaşı, karbon qazı, təbii qaz, neft, daş kömür: bunları birləşdirən nədir? |
| – | Hansı element daha çox sayda birləşmə əmələ gətirir? |
Karbon yarımqrupuna karbon C, silisium Si, germanium Ge, qalay Sn və qurğuşun Pb daxildir.
| – | С, N, O və F atomlarının xarici energetik səviyyələrinin quruluşunda ümumi cəhət nədir? |
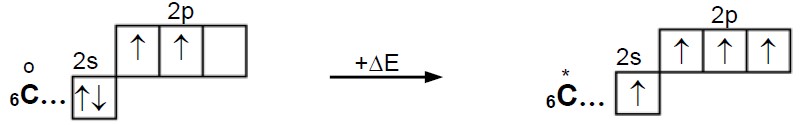
| – | Nə üçün C atomunun 2s2 elektron cütü, F, O və N atomlarının 2s2 elektron cütündən fərqli olaraq təklənə bilir? |
| – | Nə üçün karbon yarımqrupu elementlərinin ən yüksək valentlikləri eynidir və qrupun nömrəsinə bərabərdir? |
Bu elementlərin atomlarının xarici energetik səviyyəsində 4 elektron vardır: ns2np2. Ona görə də əsas yarımqrup elementləri kimi onların ən yüksək oksidləşmə dərəcəsi +4-dür. Onlar həmçinin +2 oksidləşmə dərəcəsi göstərir (SiO, CO, PbCl2, SnCl2).
C–Si–Ge–Sn–Pb sırasında elementlərin qeyri-metallıq xassəsi azalır, metallıq xassəsi artır. Bunlardan C və Si – qeyri-metal, Ge, Sn və Pb isə metaldır.
Cədvəl 32.1. Karbon və silisium elementlərinin bəzi xarakteristikaları
| Element | Valent elektronları |
Atom radiusu, nm |
Nisbi elektromənfilik |
Oksidləşmə dərəcəsi (birləşmələrində) |
| Karbon, C | 2s22p2 | 0,077 | 2,5 | –4 ÷ +4 |
| Silisium, Si | 3s23p2 | 0,117 | 1,8 | –4, +2, +4 |
Karbon
Kəşfi. Karbon qədim vaxtlardan məlumdur, kimyəvi element kimi 1775-ci ildə qəbul edilmişdir (Lavuazye, Fransa).
Dövri sistemdə mövqeyi və atomunun quruluşu. Karbon 2-ci dövr, 4-cü qrupun əsas yarımqrup elementidir. Onun atomunun elektron quruluşu 1s22s22p2-dir. Karbon atomu kimyəvi rabitələrini, əsasən, həyəcanlanmış halda əmələ gətirir və birləşmələrində IV valentli olur.